08.12.2022
Quantitative UV/VIS-Spektroskopie trüber Proben
Einleitung
Quantitative UV/VIS-spektroskopische Messungen erfordern für eine korrekte Gehaltsbestimmung das Vorliegen klarer Proben. Bei der UV/VIS-spektroskopischen Formaldehydbestimmung Wasser-basierter Dispersionsfarben nach der VdL-RL 03 [1] ist diese Voraussetzung jedoch gar nicht so selbstverständlich. Denn eine Dispersionsfarbe enthält eine relativ große Menge an Pigmenten und Füllstoffen, die ein stark streuendes opakes System darstellen - schließlich soll die Farbe ja auch ausreichend Deckkraft entfalten.
Die oben genannte VdL-Richtlinie empfiehlt die Zugabe von Acetylaceton zur unverdünnten Dispersionsfarbe, das mit evtl. vorhandenem Formaldehyd in Gegenwart von Ammoniumionen über eine Hantzsch-Reaktion eine heterozyklische Verbindung, das Diacetyldihydrolutidin (DDL), bildet (Abbildung 1) [2]. Das DDL tritt mit gelber Färbung in Erscheinung und besitzt bei einer Wellenlänge von 412 nm ein Absorptionsmaximum im UV/VIS-Spektrum.
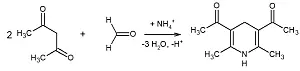
- Abb.1: Reaktionsschema zur Bildung von
Diactyldihydrolutidin (DDL) aus Formaldehyd
und Acetylaceton in Gegenwart
von Ammoniumionen.
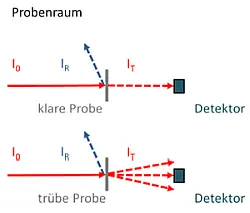
- Abb. 2: Anordnung klarer und trüber Proben
im Probenraum eines Spektrometers.
I0 kennzeichnet die Intensität der Lichtquelle
des Spektrometers, IR die Intensität
des reflektierten Anteils und IT die Intensität
des durchgelassenen Anteils.
Das Problem bei der Spektroskopie trüber Systeme besteht darin, dass die Lichtausbreitung innerhalb der Probe nicht mehr geradlinig erfolgt und das transmittierte Licht zum Teil am Detektor des Spektrometers vorbei gestrahlt wird (Abbildung 2). Die so gemessene Extinktion ist dann größer als die einer klaren Probe mit gleicher Konzentration des Analyten. Ohne entsprechende Korrektur würde man je nach Ausmaß der Trübung z.T. erhebliche Überbefunde des Analyten bestimmen.
Das im Folgenden beschriebene Korrekturverfahren geht auf Untersuchungen zur Trübung von schwach gefärbtem Humanplasma von M. Gautschi und R. Richterich zurück [3] und wird in dieser Arbeit an die Formaldehydbestimmung trüber Systeme angepasst, die mitunter eine deutliche Färbung aufweisen.
Eine weitere Möglichkeit, auch in Gegenwart einer Trübung korrekte Extinktionswerte zu erhalten, bietet die Verwendung einer ausreichend großen Integrationskugel (Ulbrichtkugel), die es erlaubt, die Küvette oder Probe im Innenraum dieser Kugel zu platzieren [4, 5]. Bei dieser Option wird neben dem transmittierten auch das gestreute Licht am Detektor empfangen, der sich wie die Probe im Innenraum der Kugel befindet. Diese Methode wird auch als Transflexionsmessung bezeichnet. Beide Verfahren werden nachfolgend diskutiert und verglichen.
Klare Lösungen
Zunächst soll der Idealfall quantitativer Gehaltsbestimmungen von Formaldehyd an klaren Lösungen mittels UV/VIS-Messungen vorgestellt werden. Platziert man derartige Systeme im Probenraum eines Spektrometers, dann fällt das durch die Probe transmittierte Licht geradlinig auf den Detektor (Abbildung 2).
Für Gehaltsbestimmungen wird die Extinktion verwendet, da diese nach Lambert-Beer der Konzentration eines Stoffes proportional ist [6]. Bei der Formaldehydbestimmung nach der VdL-RL 03 wird die Extinktion des gebildeten Diacetyldihydrolutidins (DDL) bei 412 nm herangezogen. Diese ergibt sich aus der Transmission, also dem von der Probe durchgelassenen Anteil, der direkt auf den Detektor fällt:
![]()
(Gln. 1)
mitExt: Extinktion bei 412 nm
I0: Intensität des Primärstrahls
IT: Intensität des Lichts nach dem Passieren durch die Probe
In Abbildung 3 sind die entsprechenden Spektren klarer Lösungen dargestellt, die mit einem Spektrometer mit Doppelmonochromator erhalten wurden. Doppelmonochromatoren verringern den Falschlichtanteil gegenüber Geräten mit Einfachmonochromator. Somit können auch Extinktionswerte > 1 mit geringem Fehler gemessen werden.
Der Anteil des eingestrahlten Lichts, der von der Probe in den geschwärzten Probenraum reflektiert wird und nicht auf den Detektor fällt, ist:
![]()
(Gln. 2)
mitR: Reflexion
IR: Intensität des von der Probe reflektierten Lichts
I0: Intensität des Primärstrahls
Der reflektierte Anteil einer transparenten Lösung ist relativ gering. Die Reflexionsverluste an den Luft-/Glas- bzw. Glas-/Flüssigkeits-Grenzflächen der Küvetten werden zudem über die Wasser-gefüllte Referenzküvette kompensiert.
Aus den Extinktionswerten bei 412 nm lässt sich eine Kalibriergerade für die verschiedenen Soll-Gehalte an Formaldehyd erstellen:
(Gln. 3)
mitExt: Extinktion bei 412 nm
A: Parameter
CFormaldehyd: Formaldehydkonzentration in ppm
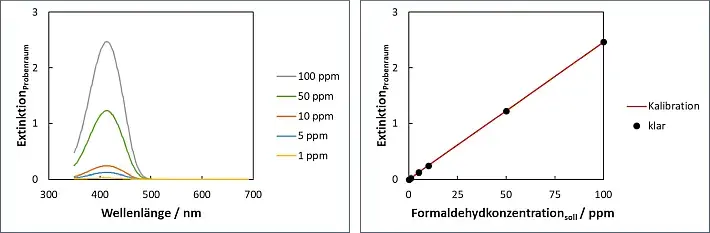
Abb.3: UV/VIS-Spektren klarer Lösungen; Formaldehydgehalte 1-100 ppm zur Kalibration; Platzierung der Küvette im Probenraum.
Abb.4: Extinktionswerte klarer Lösungen; Formaldehydgehalte 1-100 ppm zur Kalibration; Platzierung der Küvette im Probenraum.
Trübe Systeme
Die nachfolgend beschriebenen klaren Lösungen sowie die trüben Suspensionen wurden ausgehend von einer 50 ppm sowie einer 100 ppm Formaldehyd Kalibrierlösung durch Zugabe unterschiedlicher Mengen einer trüben Emulsion und anschließender Auffüllung mit VE-Wasser hergestellt. Somit konnte der Einfluss dreier gestaffelter Trübungsstufen (T1 = wenig trüb, T2 = trüb und T3 = sehr trüb) bei bekanntem Formaldehydgehalt untersucht werden.
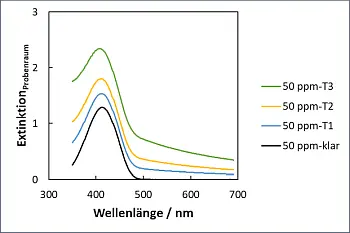
- Abb.5: UV/VIS-Spektren trüber Systeme; Formaldehydgehalten
von 50 ppm Platzierung der Küvette im Probenraum.
Wegen dieser Gesetzmäßigkeiten bietet sich ein rechnerisches Korrekturverfahren an, das die Streueigenschaften der Proben im Wellenlängenintervall 550 nm ≤ λ ≤ 690 nm, in dem die Probe nicht absorbiert, empirisch über einen Potenzansatz in Anlehnung an [3] erfasst:
(Gln. 4)
mitExtStreuung: Streukurve in Extinktionseinheiten
A: Parameter
B: Exponent
λ: Wellenlänge in nm
Für die 15 Systeme mit unterschiedlicher Trübung bei verschiedenen Formaldehydgehalten wurden einzeln die Exponenten nach Gln. 4 bestimmt. Diese streuen um einen mittleren Wert von B = -2,27 ± 0,07 und gehen im Wesentlichen auf die Teilchengröße der verwendeten Emulsion zurück, die für alle Systeme gleich ist.
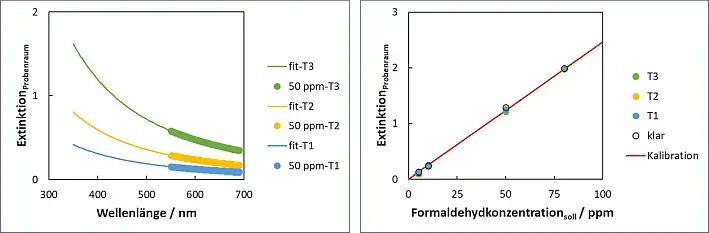
Abb.6: Rechnerisch nach Gln. 4 ermittelte Streukurven für unterschiedlich trübe Systeme mit einem Formaldehydgehalt von 50 ppm; Platzierung der Küvette im Probenraum.
Abb.7: Extinktionswerte klarer und trüber Systeme (korr. nach Gln. 4) für unterschiedliche Formaldehydgehalte mit Platzierung der Küvette im Probenraum.
Wiederfindung - Probenraum (rechnerische Korrektur)
In Tabelle 1 sind die Wiederfindungsraten aufgelistet, die mit Hilfe der beschriebenen rechnerischen Korrektur der Extinktionswerte erhalten wurden. Mit nur einer Ausnahme von -20 % (5 ppm Formaldehyd, sehr trüb) sind die Wiederfindungsraten mit ± 10 % recht gut.
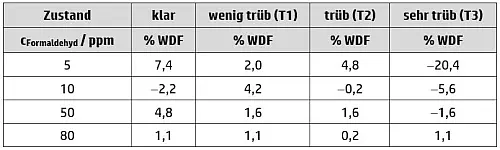
Tab.1 : Wiederfindungsraten (% WDF) für klare und verschieden stark getrübte Systeme mit unterschiedlichen Formaldehydgehalten.
Messungen im Kugelinnenraum
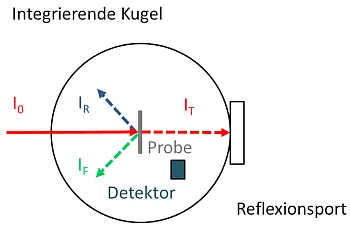
- Abb.8: Anordnung einer Probe
im Innenraum der Integrationskugel.
(Gln. 5)
mitTR: Transflexion
T: Transmission
R: Reflexion
Die Gerätesoftware ermöglicht auch eine Darstellung der Messwerte in Extinktionseinheiten, wobei zu berücksichtigen ist, dass diese scheinbare Extinktion aus zwei Beiträgen besteht, die weder die Software noch die Integrationskugel unterscheiden kann und daher nachfolgend mit einem hochgestellten Stern (*) gekennzeichnet wird:
(Gln. 6)
mitExt*: Extinktion im Kugelinnenraum bei 412 nm
TR: Transflexion
T: Transmission
R: Reflexion
Für Proben die fluoreszieren, wie es beim DDL der Fall ist [9], besteht die scheinbare Extinktion dann sogar aus drei Beiträgen:
(Gln. 7)
mitExt*: Extinktion im Kugelinnenraum bei 412 nm
T: Transmission
R: Reflexion
F: Fluoreszenz
Die Spektren der klaren Lösungen, die im Innenraum einer Integrationskugel mit hochreflektierender Innenbeschichtung platziert wurden unterscheiden sich von denen, die sich im Probenraum des Spektrometers befanden. Das verwendete Spektrometer registriert von langen Wellenlängen zu den kurzen. Dies bedeutet für das DDL, dass bei Erreichen der Anregungswellenlänge von 412 nm die Fluoreszenzemission bei ca. 510 nm ausgelöst wird und allseitig in den Kugelinnenraum abgestrahlt wird. Somit wird bei 412 nm eine geringere Extinktion erhalten als bei einer Messung von im Probenraum befindlichen Proben, da bei dieser Wellenlänge zusätzlich das Fluoreszenzlicht hinzukommt (Abbildung 9). Anschaulich ausgedrückt lässt sich der Einfluss der Fluoreszenz so beschreiben, als ob innerhalb der Kugel kurzzeitig eine Lampe eingeschaltet würde, die die Absorption verringert.
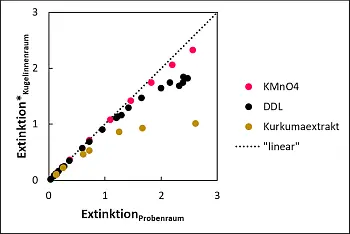
- Abb.9: Extinktionswerte verschiedener Proben,
die im Innenraum der Integrationskugel platziert waren
gegenüber denen, die sich im Probenraum befanden.
Mit zunehmender Farbstärke liegen die Extinktionswerte der in der Kugel befindlichen Proben zunehmend unterhalb derer, die im Probenraum platziert wurden. Da mit zunehmender Farbstärke die Transmission gegen Null geht - eine Extinktion von 2 im Probenraum entspricht einer Transmission von nur noch 1 % - wird die Probe opaker und im Endeffekt mehr ein Reflexions- als ein Transmissionsspektrum erhalten.
Kommt zusätzlich noch Fluoreszenz hinzu, wird die Lichtschwächung durch Absorption zunehmend durch emittiertes Fluoreszenzlicht verringert, wodurch die Extinktionswerte mehr oder weniger stark von einem linearen Verlauf abweichen. Ein solches Verhalten ist für verschiedene nicht fluoreszierende gefärbte Lösungen in An- und Abwesenheit streuender Partikel bis hin zu hohen Extinktionswerten ebenfalls berichtet worden [11].
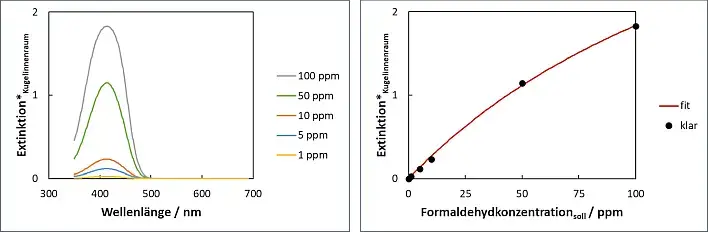
Abb.10: Spektren klarer Lösungen; unterschiedliche Formaldehydgehalte; Platzierung der Küvette im Innenraum der Integrationskugel.
Abb.11: Extinktionswerte klarer Lösungen; Formaldehydgehalte 1-100 ppm zur Kalibration, Platzierung der Küvette im Innenraum der Integrationskugel.
![]()
(Gln. 8)
mitExt*: Extinktion im Kugelinnenraum bei 412 nm
A: Parameter
B: Parameter
CFormaldehyd: Formaldehydkonzentration in ppm
Werden trübe Proben in den Kugelinnenraum eingebracht, dann unterscheiden sich deren Spektren nicht von denen klarer Lösungen, da Streulicht, reflektiertes Licht und evtl. Fluoreszenzlicht in der Kugel verbleiben und zusammen vom Detektor, der sich wie die Probe innerhalb der Kugel befindet, erfasst werden (Abbildung 12).
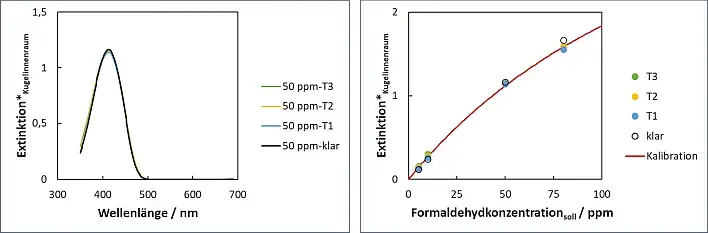
Abb.12: Spektren einer klaren sowie getrübter Lösungen für einen Formaldehydgehalt von 50 ppm
mit Platzierung der Küvette im Innenraum der Integrationskugel.
Abb.13: Extinktionswerte klarer und trüber Systeme für unterschiedliche Formaldehydgehalte
mit Platzierung der Küvette im Innenraum der Integrationskugel.
Wiederfindung - Kugelinnenraum
Die Wiederfindungsraten der Transflexionsmessungen im Kugelinnenraum (Tabelle 2) sind mit denen der Transmissionsmessungen (Tabelle 1) vergleichbar.
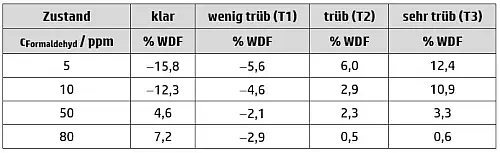
Tab.2: Wiederfindungsraten (% WDF) für klare und verschieden stark getrübte Systeme mit unterschiedlichen Formaldehydgehalten.
Fazit
Trübe Proben führen zu Überbefunden des Analyten, der bestimmt werden soll und somit zu falschen Ergebnissen, wenn die gemessenen Extinktionswerte nicht entsprechend korrigiert werden. Eine rechnerische Korrektur der Spektren trüber Proben ist mit Hilfe eines Potenzansatzes möglich und liefert überwiegend gute Wiederfindungsraten. Durch Verwendung einer Integrationskugel entsprechender Größe, die eine Platzierung der Probe im Kugelinnenraum zulässt, werden ebenfalls korrekte Extinktionswerte und gute Wiederfindungsraten erhalten. Für die untersuchten Proben können beide Methoden als gleichwertig angesehen werden.
Literatur
- VdL-Richtline 03, Richtlinie zur Bestimmung der Formaldehydkonzentration in wasserverdünnbaren Beschichtungsstoffen und Polymerdispersionen, revidierte Ausgabe Februar 2018, Verband der deutschen Lack- und Druckfarbenindustrie e.V., 1-14
- T. Nash, The Colorimetric Estimation of Formaldehyde by Means of the Hantzsch Reaction, Biochemical J. 1953, 55, 416-421
- M. Gautschi, R. Richterich, Untersuchungen zur Trübung von Humanplasma, Z. Klin. Chem. Klein. Biochem. 1973, 139-146
- B. Neumann, Klare Ergebnisse bei trüber Sicht, Farbe und Lack, 2012, 29-33
- B. Neumann, Seeing clearly through the haze, European Coatings Journal, 2015, 144-148
- W. Schmidt, Optische Spektroskopie, VCH-Verlag Weinheim, 1994, 118-119
- G. Kortüm, Reflexionsspektroskopie, Springer-Verlag, 1969, 94
- S.L. Storm, A. Springsteen, T.M. Ricker, The use of center mount sample holders in reflectance spectroscopy, 1998, Labsphere application note no. 02
- H.L.C. Pinheiro, M.V. de Andrade, P.A. de Paula Pereira, J.B. de Andrade, Spectrofluorometric determination of formaldehyde in air after collection onto silica cartridges coated with Fluoral P, Microchemical Journal 78 (1), 2004, 15-20
- Wikipedia Curcumin
- A. Mori, K. Yamashita, Y. Tabata, K. Seto, E. Tokunaga, Absorbance spectroscopy of light scattering samples placed inside an integrating sphere for wide dynamic range absorbance measurement, Rev. Sci. Instrum. 92, 2021, 123103-1-9
